保健食品注册与备案的区别
保健食品注册与备案是我国保健食品市场准入的两种管理制度,核心区别如下:
一、定义与性质差异
1. 注册
• 定义:监管部门对产品的安全性、保健功能及质量可控性进行全面技术审评,决定是否准予上市的审批过程。
• 性质:严格的行政审批,需提交毒理学、功能试验等科学依据,证明产品安全有效。

2. 备案
• 定义:企业将符合标准的产品信息提交监管部门存档备查,无需技术审评。
• 性质:形式审查,侧重材料合规性。
二、适用范围对比
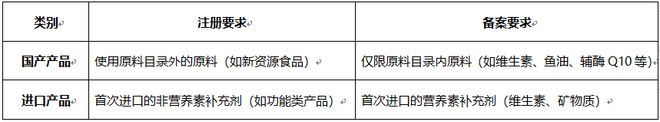
注:保健食品原料目录包含营养素补充剂、辅酶Q10、褪黑素、破壁灵芝孢子粉等10类标准化原料。
三、技术要求与材料差异
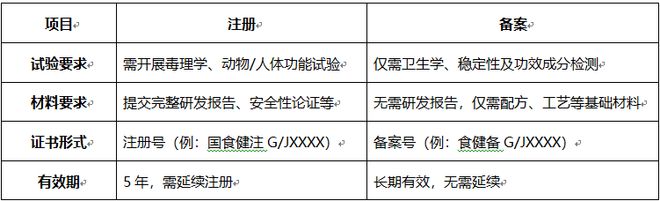
四、审批流程与周期
1. 注册流程
• 步骤:材料提交 → 技术审评(含专家评审、现场核查) → 审批发证。
• 周期:咨询专业机构。
2. 备案流程
• 步骤:材料提交 → 形式审查 → 备案公示。
• 周期:咨询专业机构。
五、监管机构
• 注册:由国家市场监督管理总局(原食药监总局)统一审批。
• 备案:国产产品由省级药监部门负责,进口产品由国家局管理。
六、如何选择注册或备案?
• 选注册:产品含新原料、新功能,或需宣称24种特定保健功能(如辅助降血脂)。
• 选备案:使用目录内原料且功能标准化(如补充维生素D)。
提示:企业需结合原料合规性、研发成本及上市周期综合决策。完整原料目录及功能清单。
以上内容综合自权威来源,如需操作细则可进一步查阅《保健食品注册与备案管理办法》。
(更多细节可参考国家市场监督管理总局官网或咨询专业机构之一 如:小蓝中康)
小蓝中康(北京)科技有限公司-保健食品研发领域领先技术服务商,为您提供保健食品研发·保健食品注册·保健食品备案·保健食品转让·保健食品延续·保健食品变更的管家式服务。
注:以上内容均由AI搜集总结并生成,仅供参考。若您期望获取专业服务,请致电400-070-1617进行咨询。
点击进入~获取专属方案,服务热线:400-070-1617、13261985261(微信同号),业务咨询












