保健食品辅料备案标准化操作流程及关键要点
保健食品辅料备案的标准化操作流程及关键要点,依据《保健食品备案可用辅料目录》及GB 2760《食品安全国家标准 食品添加剂使用标准》整理:
辅料备案全流程操作指南
1. 确认辅料是否在备案目录内
• 官方渠道核查
登录国家市场监督管理总局官网 → 进入“保健食品备案信息系统” → 查询最新《保健食品备案可用辅料目录》(2025年更新版)。
注意:目录外辅料需按新原料申报(流程复杂且周期长达2-3年)。

2. 核查用量是否符合GB 2760
• 限量标准
o 对照GB 2760中辅料的允许使用范围、最大使用量及残留量(如硬脂酸镁在片剂中限量为0.15g/kg)。
o 复合辅料需拆分验证各组分合规性(如羟丙甲纤维素中含钛白粉需单独核算)。
• 特殊限制
o 婴幼儿保健食品禁用:人工色素(如柠檬黄)、防腐剂(苯甲酸)等。
3. 验证辅料功能中性(无保健声称)
• 禁用行为
o 辅料不得在标签或说明书中标注功能效果(如“微晶纤维素促进吸收”属违规)。
• 工艺必要性证明
o 需提供文件说明辅料仅用于工艺目的(如:硬脂酸镁:改善压片流动性;胶原蛋白:不可仅作为填充剂(因其有功能暗示))。
4. 准备工艺必要性说明
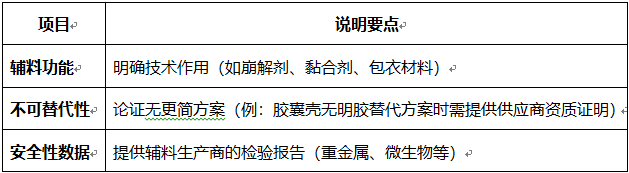
• 核心内容要求
5. 提交备案材料清单
• 必需文件
o 辅料合规声明(加盖企业公章)
o GB 2760符合性计算表(附公式及数据来源)
o 工艺流程图(标注辅料添加节点及目的)
o 辅料供应商的《食品生产许可证》及批次检验报告
常见驳回风险与规避策略

特殊情形处理
1. 进口辅料
o 需额外提交:出入境检验检疫证明、原产地安全标准(需等同于GB 2760)。
2. 目录外辅料
o 申请新辅料注册:提交毒理学试验(急性+亚慢性毒性)、功能必要性论证(3家机构背书)。
备案周期:材料齐全后在规定的工作日完成。
总结
辅料备案的核心是合规性+工艺必要性证明。企业需:
1. 严格限定辅料在目录内且符合GB 2760;
2. 彻底剥离辅料与功能声称的关联;
3. 建立供应商审查机制。
建议借助专业机构(如小蓝中康)的备案加速服务,避免因细节瑕疵延误上市计划。
小蓝中康(北京)科技有限公司-保健食品研发领域领先技术服务商,为您提供研发·注册·备案·转让的管家式服务。
注:以上内容均由AI搜集总结并生成,仅供参考。若您期望获取专业服务,请致电400-070-1617进行咨询。
点击进入~获取专属方案,服务热线:400-070-1617、13261985261(微信同号)保健食品研发申报












