保健食品注册难不难?关键要点汇总给您看!
保健食品注册流程及关键要点
一、注册流程概览
1. 前期准备
o 功能定位:明确产品功能(如抗氧化、增强免疫力等),作为配方研发和原料选择的基础。
o 配方论证与样品制备:根据功能需求确定配方可行性,完成研发后生产三批次中试样品用于检测。

2. 材料准备
o 核心材料:包括注册申请表、产品研发报告、配方及工艺说明、安全性评估(毒理学)、功能性评估(功能学试验/人体试食试验)、标签说明书样稿、样品检验报告等。
o 特殊要求:进口产品需额外提交生产国资质证明、出口国上市证明等。
3. 提交申请与形式审查
o 提交途径:注册产品及进口产品直接报国家市场监督管理总局。
o 审查时间:受理机构在规定的工作日内完成形式审查,材料不完整需补正。
4. 技术审评与现场核查
o 技术审评:审评机构评估安全性、功能有效性及质量可控性,周期咨询专业机构,可能要求补充材料。
o 现场核查:重点检查生产条件、工艺流程及质量管理体系,需动态生产并抽样复核。
5. 审批与证书颁发
o 审批决定:通过后20个工作日内颁发《保健食品注册证书》,有效期5年。
o 文号格式:国产为“国食健注G+年份+顺序号”,进口为“国食健注J+年份+顺序号”。
6. 后续监管
o 延续注册:需在证书到期前6个月申请,逾期可能导致注销。
o 变更管理:涉及配方、工艺等重大变更需重新申报,注册期间不可同步转让技术。
二、关键要点及注意事项
1. 材料合规性
o 原料种类、生产工艺不得擅自更改,技术要求需符合现行法规。
o 所有文件需电子化提交(PDF格式),外文材料需翻译并公证。
2. 特殊情形处理
o 注册转备案:若原料被纳入保健食品目录,需转为备案管理。
o 证书遗失:需提交遗失声明及情况说明。
o 变更及转让:需提交变更或转让申请,经审评审批。
3. 时间与费用
o 周期:国产注册、进口产品等申报周期咨询专业机构。
o 费用:包括研发费、检测费、注册费。
4. 风险提示
o 常见驳回原因:材料不全(如缺生产销售证明)、技术要求不符、功能验证不充分。
o 动态合规:获批后需持续监控质量,定期提交不良反应报告。
三、注册与备案的区别
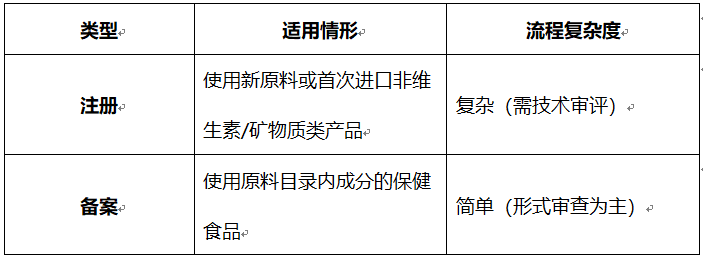
提示:企业可参考国家市场监督管理总局官网获取最新模板,并咨询省级监管部门确认地方性要求。
注:以上内容均由AI搜集总结并生成,仅供参考。若您期望获取专业服务,请致电400-070-1617进行咨询。
点击进入~获取专属方案,服务热线:400-070-1617、13261985261(微信同号)












