保健食品申报路径及流程解析
保健食品的申报主要有“注册”与“备案”两种路径,具体走哪条取决于产品使用的原料是否在官方目录内。下面这个表格可以帮你快速了解两者的核心区别。
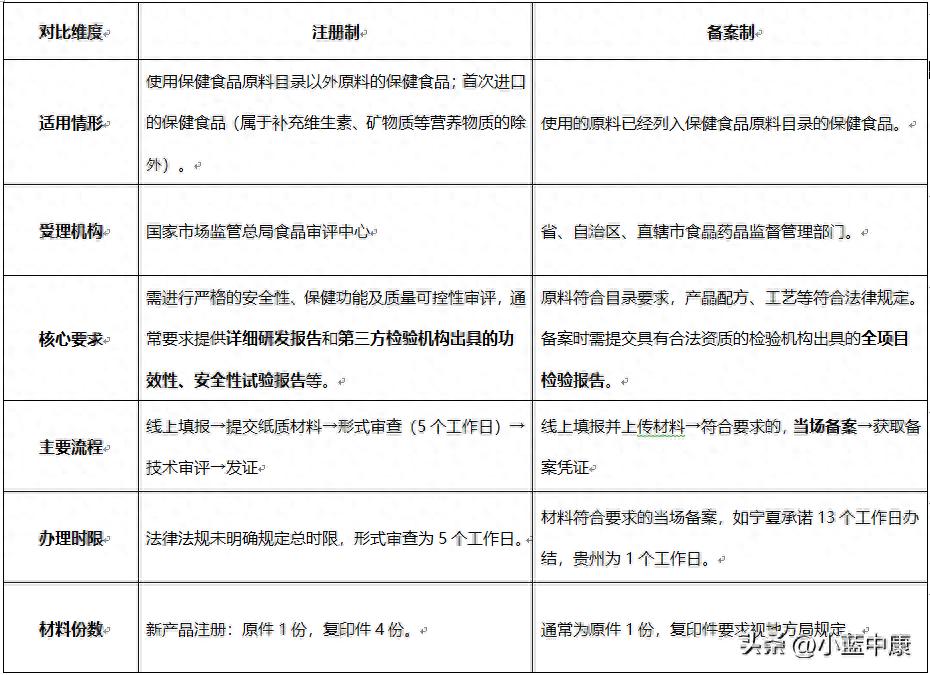
申报路径选择与详细流程
1. 注册制
如果你的产品不符合备案制的要求,就需要申请注册。整个流程中,材料的准备至关重要。
· 关键材料准备:
o 安全性评价材料:需由法定检验机构出具安全性评价试验报告。
o 保健功能评价材料:需由法定检验机构出具保健功能评价试验报告。如果涉及人群食用评价,报告需为原件,并在有效期内。
o 产品配方与生产工艺材料:提供原料和辅料的名称及用量、生产工艺流程等。
o 产品技术要求材料:包括感官要求、理化指标、微生物指标等。
· 形式审查与受理:无论通过受理大厅前台还是邮件递交材料,形式审查时间均为5个工作日。审查通过后,会获得《受理通知书》。
· 技术审评与补充材料:技术审评阶段,审评部门可能会提出补正意见。你需要在收到《审评意见通知书》后3个月内一次性提交全部补充材料。
· 时限提醒:
o 延续注册:需在保健食品注册证书有效期届满6个月前提出并获准受理。
o 材料有效期:涉及批件有效期、检验报告有效期等有时限要求的材料,递交时间以纸质材料到达受理大厅的时间为准。务必提前安排,避免逾期。
2. 备案制
备案制适用于使用已列入保健食品原料目录的原料生产保健食品。
· 核心优势:流程大大简化,办理速度非常快。
· 基本流程:通过各地的政务服务网在线提交备案材料,例如“保健食品备案管理信息系统”。材料符合要求即可当场备案。
· 所需材料:主要包括保健食品备案登记表、备案人主体登记证明文件、产品配方材料、产品生产工艺材料、产品技术要求材料、全项目检验报告等。
实用建议与常见问题
· 提前规划与预留时间:特别是注册制,从准备材料到最终获批周期较长,务必为检验、材料准备和审评补正留出充足时间。
· 注重材料细节:
o 申请材料应使用A4纸打印,中文一般不小于宋体小四号字。
o 整套材料需装订成册,各项材料之间使用明显的区分标志。
o 除注册申请表和检验报告等特定文件外,申请材料应逐页或骑缝加盖申请人公章。
o 申请表中法定代表人的签字必须是亲笔签名,不能使用签名章或扫描件。
· 善用咨询渠道:申报前可充分利用官方提供的咨询渠道,如电话咨询、现场咨询等,提前解决疑问,能有效提高申报成功率。
希望以上信息能帮助你理清保健食品申报的思路。如果你能告知产品具体使用的原料,我可以帮你进一步判断它更适合注册还是备案路径。
(更多细节可参考国家市场监督管理总局官网或咨询专业机构之一如:小蓝中康)
小蓝中康(北京)科技有限公司-保健食品研发领域领先技术服务商,为您提供保健食品研发·保健食品注册·保健食品备案·保健食品转让注册·保健食品延续注册·保健食品变更注册等的管家式服务。
注:以上内容均由AI搜集总结并生成,仅供参考。若您期望获取专业服务,请致电400-070-1617进行咨询。
点击进入~获取专属方案,服务热线:400-070-1617、13261985261(微信同号)业务咨询












