保健食品申报全流程解析:保健食品注册与保健食品备案制
保健食品的申报流程主要依据国家市场监督管理总局发布的《保健食品注册与备案管理办法》及相关配套法规执行。流程分为注册制和备案制两大类,具体路径取决于产品使用的原料、功能声称等因素。以下是核心流程的详细说明:
一、 判定申报路径(注册 or 备案)
1. 需注册的情形
• 使用不在《保健食品原料目录》内的原料
• 首次进口的保健食品(属于补充维生素矿物质等备案产品的除外)
• 声称具有特定保健功能且不在备案范围内的产品
• 原料或功能涉及安全性与科学性需深入验证的产品

2. 可备案的情形
• 使用的原料及用量均在《保健食品原料目录》内
• 符合目录规定的生产工艺标准
• 声称的功能在目录允许范围内(目前主要是补充维生素、矿物质类)
• 国产或已取得进口备案凭证的再次进口产品
二、 保健食品注册流程
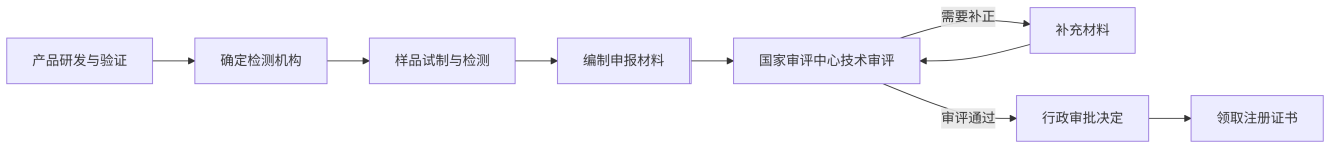
1. 前期研究与验证
• 配方依据:传统养生理论或科学文献支撑
• 工艺研究:确定生产工艺稳定性
2. 样品生产与检测
• 在符合GMP标准的车间试制3批次样品
• 委托国家认证的检测机构(如各省市药检所)进行:
• 卫生学试验(重金属/微生物等)
• 功效成分检测
• 安全性评价:急性/遗传毒性试验(必需)
• 功能性验证:动物或人体试验(依功能而定)
• 稳定性试验:保质期内功效成分留存率验证
3. 国家审评与技术核查
• 材料提交至 国家市场监督管理总局食品审评中心
• 审评中心组织专家评审:
• 配方合理性
• 工艺可行性
• 安全性/功能声称证据强度
• 现场核查:随机抽查生产线与质量管理体系
4. 补充资料与审批发证
• 针对审评意见补充材料(只有1次机会)
• 通过后颁发《国产/进口保健食品注册证书》(有效期5年)
三、 保健食品备案流程(简化程序)
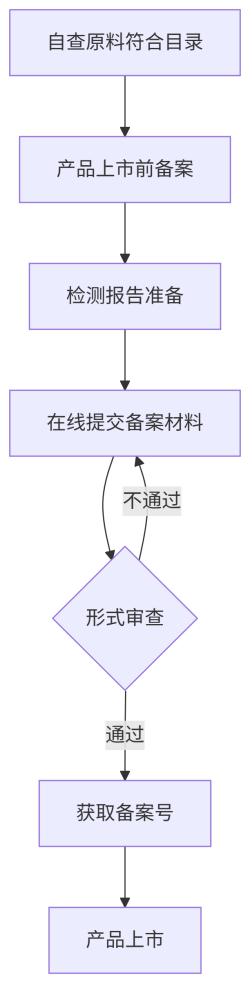
1. 自查合规性
• 确认所有原料及用量均在《保健食品原料目录》内
• 核对生产工艺是否符合目录要求
2. 产品检测与材料准备
• 提供卫生学、功效成分及稳定性检测报告
• 编制备案表、说明书、产品质量标准等
3. 在线备案与公示
• 通过 “保健食品备案信息系统” 提交材料
• 监管部门完成形式审查
• 公示备案信息并发放备案号(格式:食健备G/J+年份+编号)
四、 关键注意事项与趋势
1. 合规重点
• 标签规范:不得暗示治疗作用,需标注“保健食品不是药物”
• 功能声称:严格限定在24种允许范围内(如有助于增强免疫力、有助于抗氧化、辅助改善记忆、缓解视觉疲劳、清咽润喉、有助于改善睡眠、缓解体力疲劳、耐缺氧、有助于控制体内脂肪、有助于改善骨密度、改善缺铁性贫血、有助于改善痤疮、有助于改善黄褐斑、有助于改善皮肤水份状况、有助于调节肠道菌群、有助于消化、有助于润肠通便、辅助保护胃粘膜、有助于维持血脂(胆固醇/甘油三酯)健康水平、有助于维持血糖健康水平、有助于维持血压健康水平、对化学性肝损伤有辅助保护作用、对电离辐射危害有辅助保护作用、有助于排铅)
• 原料管理:新原料需单独申报,评审周期更长
2. 2025年新动向
• 目录持续扩增:人参、灵芝等传统原料正推进纳入备案目录
• 电子化提速:注册流程逐步迁移至线上系统
• 监管趋严:对虚假功能宣称的处罚力度加大
五、 获取官方支持
• 法规查询:国家市场监督管理总局官网 → 特殊食品信息查询平台
• 检测机构名单:认监委公布的《食品检验机构资质认定名录》
• 专业服务建议:委托具有保健食品研发经验的申报机构
提示:若产品定位尚未明确,建议优先选择备案目录内原料开发,可节省至少18个月上市时间。2024年新纳入目录的黄芪、西洋参等原料正成为企业布局热点。
申报过程实质是企业研发能力与合规水平的双重考验,建议前期投入充分资源进行配方论证,避免后期因技术缺陷导致退审,既延误商机又增加成本。
(更多细节可参考国家市场监督管理总局官网或咨询专业机构之一如:小蓝中康)
小蓝中康(北京)科技有限公司-保健食品研发领域领先技术服务商,为您提供研发•注册•备案•转让•延续•变更的管家式服务。
注:以上内容均由AI搜集总结并生成,仅供参考。若您期望获取专业服务,请致电400-070-1617进行咨询。
点击进入~获取专属方案,服务热线:400-070-1617、13261985261(微信同号)业务咨询












